PNAS | 我院干细胞与动物疾病团队以长文揭示维持哺乳动物干细胞多能性的关键超级增强子
9月26日,我院干细胞与动物疾病团队、生命科学院廖明帜和北京生命科学研究所王伟团队合作在 PNAS 杂志在线发表题为“Super-enhancers conserved within placental mammals maintain stem cell pluripotency”(DOI number 10.1073/pnas.2204716119)的研究论文。
超级增强子(Super-enhancer, SE)被认为是细胞命运决定、多能性维持和疾病发生的主要调控中枢。但是,与多能性相关的超级增强子在哺乳动物中的进化规律一直没有得到阐明,是否存在维持干细胞多能性的关键超级增强子尚不清楚。该研究通过多组学技术对人、猪和小鼠的超级增强子的系统比较,揭示了大多数超级增强子在哺乳动物中经历了快速进化,并鉴定出SOX2、PIM1、FGFR1等3个维持胎盘哺乳动物多能性的关键超级增强子。该研究为理解哺乳动物多能性调控机制提供了新见解,为进一步提高多能性干细胞建系效率和促进大动物多能性干细胞的应用奠定了基础。
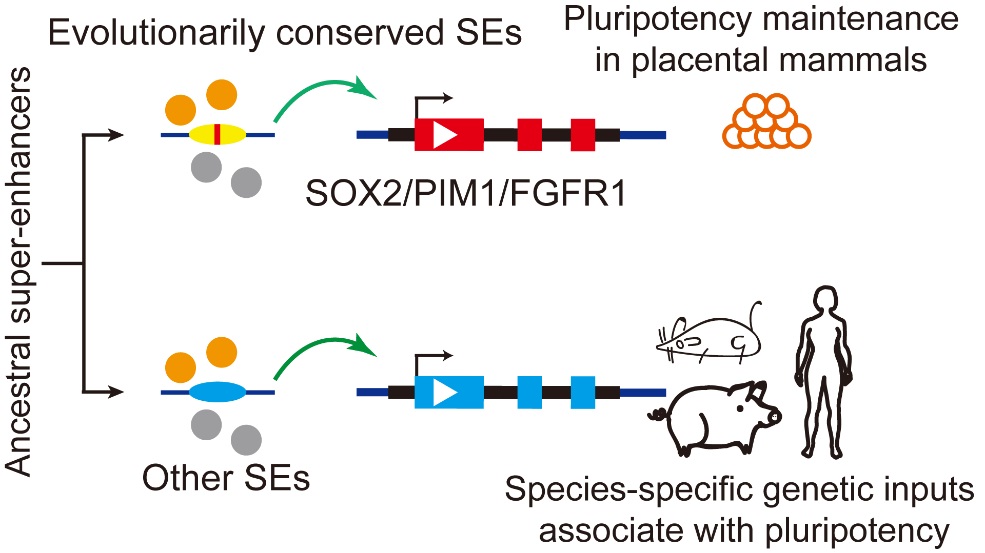
图1哺乳动物多能性相关SEs的进化模型
大量研究表明,哺乳动物共享相同的核心重编程因子,如OCT4和SOX2。然而,哺乳动物不同物种多能干细胞的维持依赖明显差异的外部信号。这种差异背后的遗传机制在该领域仍然是一个悬而未决的关键科学问题。顺式调节元件或增强子的进化变化被认为是决定物种多样性的重要来源。一个令人兴奋的假设是,作为核心转录因子在基因组的主要结合位点,大量哺乳动物多能性相关SE经历了快速进化,帮助形成多能性相关网络的物种特异性调节机制。与此同时,少部分关键SE被保留下来,以维持哺乳动物干细胞的多能性。
为了验证这一科学假设,该研究在人、猪和小鼠的多能干细胞中进行了全面的表观基因组和转录因子多组学整合分析,鉴定出人、猪和小鼠的多能性相关的SEs,并确定BRD4对多能性相关超级增强子功能的维持是必须的。分子系统发育分析结果表明,尽管这些多能性相关的SEs可以募集相似的转录因子,然而大多数的SEs序列发生了快速的进化。随后,SOX2、PIM1、FGFR1等三个在胎盘动物基因组中高度保守的SEs被首次鉴定出来,这些物种间高度保守的SEs可以在多能干细胞中驱动下游报告基因的表达,并且在细胞分化或添加BRD4的抑制剂后失活。通过CRISPR/Cas9方法破坏这些高度保守的SEs严重损害了干细胞的多能性,表明这些序列保守的SEs在胎盘动物多能干细胞的维持中发挥着关键作用,而与多能性相关的SEs在不同物种的序列变化可能阐明和揭示维持干细胞多能性的外部信号的不同需求。这项研究将深入促进哺乳动物多能性维持机制的研究。
我院干细胞与动物疾病团队的华进联、李娜,生命科学院廖明帜,北京生命科学研究所的王伟为本文的通讯作者。我院博士研究生张炬庆与生命学院的硕士研究生周亚琦为本文的第一作者。
本研究受到国家自然科学基金、国家重大研发计划、陕西省重点科技创新团队和陕西省重点研发计划等项目资助。
原文链接:www.pnas.org/doi/10.1073/pnas.2204716119